|
разместить свою ссылку>>
__________________________________
если Ваш сайт содержит материалы
по этой теме, Вы можете
бесплатно разместить здесь свою
ссылку или баннер. |
|
|
|
1.
В.ОЛЬШАНСКИЙ.
АЛЕССАНДРО ВОЛЬТА И ЛУИДЖИ ГАЛЬВАНИ: НЕОКОНЧЕННЫЙ СПОР.
Оцифровано: журнал Наука и Жизнь Ж12 2004.
Рубрика "Исторические миниатюры".
WITTE 0. A. THE
AUTOMOBILE STORAGE BATTERY ITS CARE AND REPAIR.
Published 1922 by THE AMERICAN BUREAU
OF ENGINEERING, INC. CHICAGO, ILLINOIS, U. S. A.
В популярной форме изложена
теория и практика промышленного изготовления
электрохимических батарей и аккумуляторов.
rar-архив html-версии
книги (в сумме 9 Мб на английском).
Советую прочесть!
часть1>>>
часть2>>>
|
|
|
|
|
|
|
В этом разделе приводятся описания
существовавших ранее и применяющихся в настоящее
время химических источников постоянного тока,
советы и статьи по их изготовлению, а так же
дополнительный материал, который несомненно
будет полезен всем интересующимся.
История
развития гальванических элементов легко
прослеживается из следующей таблицы:
|
Годы |
Автор |
Открытие или изобретение |
| 1789 |
Гальвани |
Опыты с
физиологическим действием тока |
| 1794 |
Вольта |
Первый
гальванический элемент |
| 1800 |
Вольта |
Вольтов
столб и первая батарея из элементов |
| 1833 |
Грове |
Первое
применение деполяризатора |
| 1836 |
Даниель |
Введение
принципа упругостей растворения металлов |
| 1841 |
Бунзен |
Хромовый
деполяризатор |
| 1859 |
Мейдингер |
Техническое применение элементов -
телеграф |
| 1865 |
Лекланше |
Применение перекиси марганца и
хлористого аммония |
| 1879 |
Меш |
Применение деполяризации кислородом
воздуха |
| 1882 |
Лаланд |
Применение окиси меди и щелочного
электролита |
| 1888 |
Гаснер |
Сухой
элемент |
| 1914 |
Фери |
Техническое применение воздушной
деполяризации |
Описания химических источников тока: |
|
Элемент
Даниэля
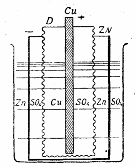
Zn+CuSO4 = Cu+ZnSO4
1,1 v
|
Хромокисный элемент
(элемент
Гренэ)
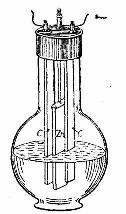
3Zn+2CrO3+6H2SO4
=
Cr2(SO4)3+3ZnSO4+6H2O
2,0 v |
Элемент
Бунзена
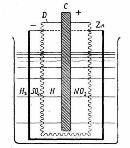
|
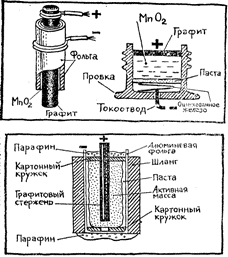
Элемент Лекланше
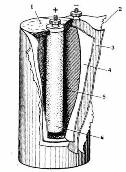
Zn+2NH4Cl+2MnO2 = ZnCl2+Mn2O3+2NH3+H2O
1,5 v
Существовало и существует
большое количество модификаций |
|
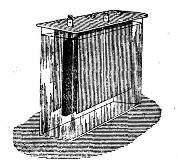
Элемент
Лаланда
 |
Элемент Мейдлингера
(разновидность элемента Даниэля)

Zn+CuSO4 = Cu+ZnSO4
1,1 v
|
Элемент
Фери

Zn+H2O+O
= Zn(OH)2
1,25
v |
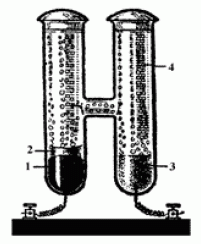
Нормальные элементы Кларка:
Zn+Hg2SO4=ZnSO4+2Hg
1,433
v при 15 0С
и Вестона:
Cd+Hg2SO4=CdSO4+2Hg
1,0184 v
при 20 0С
 |
| |
|
|
|
|
Химические
и не только источники тока своими руками: |
|
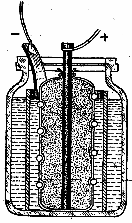
Элемент Лекланше своими
руками
 |
Переменнотоковый
гальваничесий элемент.
Скорее занимательный опыт, чем действующий
гальванический элемент, но почитать полезно.
 |
Свинцово-поташный
аккумулятор
 |
|
Электростанция в рюкзаке
 |
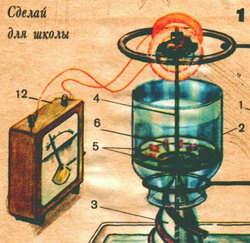
Настольная
гидроэлектростанция
 |
|
|
Совсем
простой ХИТ
 |
Постройка газового аккумулятора
 |
Источники
тока из подручных средств
 |
|
|
|
|
|
|
Много
интересного по этой и другим темам, можно почитать в
журнале "Юный техник". Если бумажного варианта в наличии
у Вас нет, можно порыться в электронной библиотеке
журнала
www.jt-arxiv.narod.ru
|
|
|
|
|