Предыдущая Следующая
РО43
– + Н2О↔НРО42 – + ОН-
равна
КВ
10 – 14
Кr = = = 7,7 •10 –3
КД,3
7,3 •10 – 12
Гидролиз солей, образованных сильной
кислотой
и слабым основанием, напримерNH4C1. В растворе соль NH4Cl диссоциирована
NH4C1
→ NH4+ + С1 –
Гидролизу подвергается ион слабого основания NH4+
NH4+
+ Н2О↔NH4OH + H+
Как видно, в результате
гидролиза соли появляется некоторое избыточное количество ионов водорода, т. е. среда подкисляется. Таким образом, гидролиз
соли, образованной сильной кислотой и слабым основанием, приводит к подкислению
раствора.
Степень гидролиза и
константа гидролиза в данном случае описываются теми же уравнениями, но лишь
с включением константы диссоциации слабого основания.
Равновесную концентрацию ионов водорода
можно вычислить из уравнения:
[Н+] =
βс = 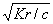
Соответственно
водородный показатель среды рассчитывается по уравнению:
РН = -1g[Н+] = -
1g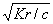 = -1g = -1g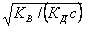
Гидролиз соли, образованной слабым основанием
и слабой кислотой, напримерNH4F
NH4F →
NH4+ + f-
NH4+
+ H2O↔NH4OH + H+
F - + Н2О↔
HF + OH –
Как видно,
в результате гидролиза образуются как ионы водорода, так и ионы гидроксида. Константа гидролиза зависит от константы
диссоциации как слабого основания КД,О, так и слабой кислоты КД,К
КВ
Кr =
КД,К КД,О
Степень
гидролиза и концентрация ионов водорода в этом случае не зависят от исходной концентрации соли:
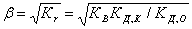
[H+] =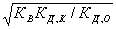
рН=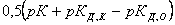
Как видно,
в зависимости от соотношения рКД,К и рКД,О среда
может иметь как кислую, так и основную
реакцию.
Предыдущая Следующая
|