Предыдущая Следующая
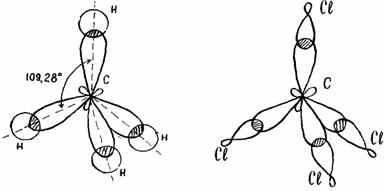
Другие примеры гибридизации: BeH2(sp-),
BF3 (sp-2), РСl5(sp3d-)
и др.
На гибридных орбиталях, как и на
обычных орбиталях, может располагаться не только по одному электрону,
но и по два. Например, четыре sp3-гибридные орбитали атома кислорода
О таковы, что две из них содержат по паре электронов, а две – одному
неспаренному электрону. С современных позиций строение молекулы
воды рассматривается с учетом гибридизации орбиталей атома О и тетраэдрической структуры
молекулы Н2O в целом.
4.5. Метод
молекулярных орбиталей (ММО, МО). Хронологически
метод МО появился позже метода ВС, поскольку оставались в теории ковалентной связи
вопросы, которые не могли получить объяснение методом ВС. Укажем некоторые из
них.
Как известно, основное
положение метода ВС состоит в том, что связь между атомами осуществляется за
счет электронных пар (связующих двухэлектронных облаков).
Но это не всегда так. В ряде случаев в образовании химической связи участвуют отдельные
электроны. Так, в молекулярном ионе Н2+ одноэлектронная связь.
Метод ВС образование одноэлектронной связи объяснить не
может, она противоречит его основному положению.
Метод ВС не объясняет также роли неспаренных электронов в молекуле. Молекулы,
имеющие неспаренные электроны, парамагнитны,
т. е. втягиваются в магнитное поле, так как неспаренный электрон
создает постоянный магнитный момент. Если в молекулах нет неспаренных электронов,
то они диамагнитны – выталкиваются из магнитного
поля. Молекула кислорода парамагнитна, в ней имеется два электрона
с параллельной ориентацией спинов, что противоречит методу ВС. Необходимо также
отметить, что метод ВС не смог объяснить ряд свойств комплексных соединений – их
цветность и др.
Чтобы объяснить эти факты, был
предложен метод молекулярных орбиталей (ММО).
4.5.1. Основные положения
ММО, МО.
1. В молекуле все электроны являются
общими. Сама молекула — это единое целое, совокупность ядер и электронов.
2. В молекуле каждому электрону
соответствует молекулярная орбиталь, подобно тому как каждому
электрону в атоме соответствует атомная орбиталь. И обозначения орбиталей аналогичны:
АО s, p, d, f
Предыдущая Следующая
|