Предыдущая Следующая
является константой диссоциации КД
слабой кислоты НА. Таким образом, константа гидролиза равна отношению ионного произведения воды и константы
диссоциации слабого электролита:
Кr = КВ / КД
Если выразить
концентрацию ионов и молекул при установлении равновесия
СН3СОО
– + Н2О ↔
СН3СООН + ОН –
через степень гидролиза β и исходную
концентрацию иона с, то получаем,
что
[СН3СООН] =
[ОН –] = βс, а
[СН3СОО –] = (1 - β)с
Подставив эти значения в уравнение
[НА][ОН–]
Кr =
[А–]
получим:
Кr = КВ/КД = β2с
/ ( 1 - β).
Если β « 1,то
Кr = β2с
Отсюда
следует, что

Как видно,
степень гидролиза возрастает с уменьшением концентрации гидролизующегося иона. По уравнению Кr = β2с можно найти равновесную концентрацию гидроксид-иона:
[ОН-] = βс
= 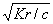
и рОН = -lg[OH-] = -lg 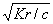 = - lg = - lg 
Отсюда
легко вычисляется рН раствора соли
рН = рКВ - рОН = рКВ -lg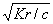
Если гидролизу
подвергается многоосновной анион, то гидролиз протекает по стадиям:
СО32-
+ Н2О↔НСО3– +ОН –
НСО3
– + Н2О ↔ Н2СО3 + ОН–
Константа
гидролиза по первой ступени значительно выше, чем константа гидролиза по последней ступени. Например, для гидролиза СО32
– , при 298 К
Кr1 = 2•10 – 4 ; Кr2 = 2,2-10 – 8
Поэтому,
при расчете концентраций ионов [ОН–] или [Н+], второй
и третьей ступенью гидролиза обычно пренебрегают.
Анализ уравнений гидролиза показывает, что в уравнении Кr = КВ / КД для расчета
константы гидролиза по первой ступени входит константа диссоциации слабого электролита
по последней ступени. Например, константа
гидролиза иона СО32- по первой ступени
СО32
- + Н2О↔ НСО3– + ОН –
равна
КВ
10 – 14
Кr = = = 2 •10 – 4
КД,2 4,8 •10 – 11
а константа
гидролиза иона РО43 – по первой ступени
Предыдущая Следующая
|